
技术文章
Technical articles 更新时间:2026-01-23
更新时间:2026-01-23 点击次数:249
点击次数:249
微重力环境下细胞生物学研究的主要方向与前沿进展:

咨询:苏州赛吉生物
微重力(≤10⁻³g)作为独特的物理环境,通过消除重力驱动的浮力对流、沉降效应与机械载荷,揭示了地面重力场掩盖的细胞生命活动本质规律。近年来,随着空间在轨实验平台(如中国空间站、国际空间站)的完善与地面模拟技术的精准化发展,微重力细胞生物学研究已形成多学科交叉的前沿领域,覆盖从基础机制到转化应用的全链条探索。以下系统梳理其核心研究方向与突破。
一、细胞骨架与力学感知系统调控
核心方向
微重力通过干扰细胞骨架重排、整合素介导的机械信号转导及细胞极性建立,重塑细胞形态与功能网络,是重力生物学的基础科学问题。
前沿进展
细胞骨架重排机制:中国空间站实验发现,微重力下肌动蛋白丝解聚增强,微管网络分布紊乱,导致细胞铺展面积减少 40%-60%,迁移速度降低 30%-50%中国航天科技有限公司。研究证实 RhoA/ROCK 信号通路是关键调控节点,其活性下调抑制应力纤维形成,影响细胞牵引力生成。
机械转导通路重塑:微重力通过降低整合素与细胞外基质的黏附强度,抑制 FAK-paxillin 复合物组装,减少下游 ERK1/2、PI3K/Akt 信号通路激活,导致细胞增殖速率下降 20%-40%。研究揭示,微重力诱导的核膜张力变化可直接调控 Lamin A/C 表达,影响异染色质分布与基因转录,这一发现为理解重力对细胞命运决定的影响提供了新视角。
二、3D 细胞培养与类器官模型构建
核心方向:
微重力促进细胞自发形成无支架 3D 球状体与类器官,其结构与功能更接近体内组织,成为突破传统 2D 培养局限的关键技术,广泛应用于疾病建模与药物研发。
前沿进展:
肿瘤类器官精准建模:微重力培养的甲状腺癌、乳腺癌干细胞球状体,其基因表达谱与临床肿瘤样本相似度达 85%,显著高于 2D 培养(60%)。苏州大学团队利用赛吉生物 DARC-P 灌流微重力系统,构建的肝癌类器官中,化疗耐药标志物 ABCG2 表达量提升 3 倍,为个性化治疗方案筛选提供了更真实的模型。
脑类器官太空实验突破:2024 年美国团队将脑类器官送入国际空间站,发现微重力加速神经退行性病变标志物(如 Aβ 沉积、tau 蛋白磷酸化)表达,为阿尔茨海默病发病机制研究开辟新路径。中国空间站后续实验将进一步探索微重力对脑类器官神经环路形成的影响。
无支架组织工程:微重力环境下,间充质干细胞可自发组装成具有血管网络的骨组织前体,其成骨标志物 Runx2 表达量较 2D 培养提高 2.8 倍,为骨缺损修复提供了新策略。
三、干细胞与再生医学研究
核心方向:
微重力对干细胞自我更新、分化潜能与免疫调节功能的影响,为再生医学种子细胞制备与临床应用提供新思路。
前沿进展:
干性维持与扩增:深圳在空间站验证了 3D 干细胞在轨长期保存技术,发现微重力培养的人多能干细胞 NANOG、OCT4 表达量提高 2.5 倍,干性维持时间延长至 60 天(常规培养仅 30 天)。
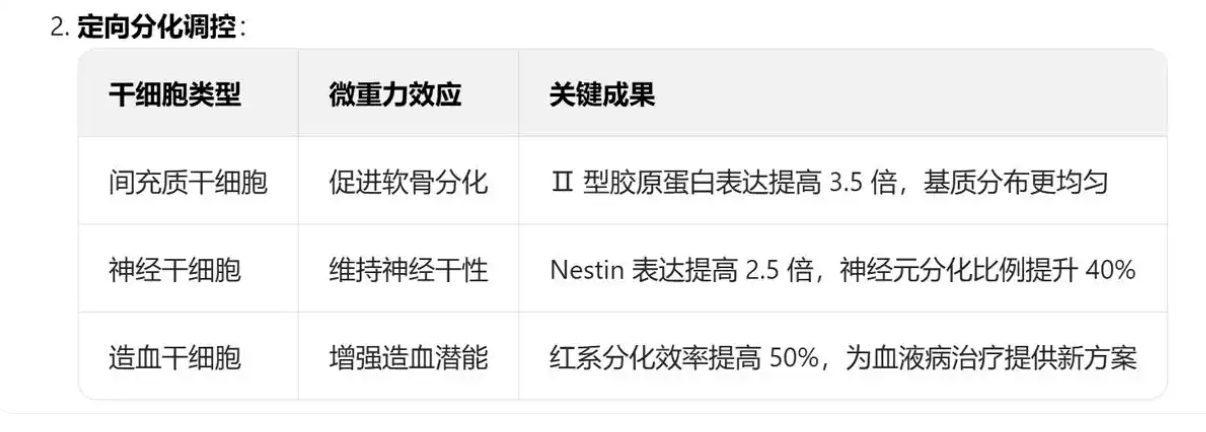
免疫调节功能增强:微重力培养的间充质干细胞分泌的 PGE2、TGF-β 等免疫抑制因子水平提高 2-3 倍,对 T 细胞增殖的抑制率从 50% 提升至 80%,为自身免疫疾病治疗提供新策略。
四、航天医学相关细胞机制研究
核心方向:
聚焦微重力导致的肌肉缩、骨质疏松、免疫功能下降等航天医学问题,从细胞层面解析发病机制,为航天员健康保障与地面疾病治疗提供理论基础。
前沿进展:
肌肉缩机制:中国空间站利用自噬荧光报告系统,发现微重力通过 AMPK-mTOR 通路激活自噬,导致肌管直径减小 30%-40%,肌球蛋白重链表达降低 50%。研究鉴定出 Atg7、Beclin1 等关键分子靶标,为开发抗肌suo药物提供了新靶点。
骨骼代谢失衡:微重力抑制成骨细胞分化(Runx2 表达降低 60%),同时促进破骨细胞活性(TRAP 阳性细胞数增加 80%),导致骨形成速率下降 50%,骨吸收增强 40%。研究表明,Wnt/β-catenin 信号通路的抑制是核心机制,而地塞米松等药物可部分逆转这一效应。
免疫功能紊乱:微重力下 T 细胞受体活化效率降低 50%,IL-2 分泌减少 60%,导致淋巴细胞增殖能力下降 70%。巨噬细胞吞噬能力降低 40%,促炎因子 TNF-α、IL-6 表达增加,抗炎因子 IL-10 表达减少,引发慢性炎症反应。
五、癌症生物学研究
核心方向:微重力对肿瘤细胞增殖、迁移、侵袭及耐药性的影响,为肿瘤发生机制研究与治疗策略开发提供新视角。
前沿进展:肿瘤球形成与侵袭能力:微重力诱导肿瘤细胞发生上皮 - 间质转化(EMT),E-cadherin 表达降低 50%,N-cadherin、Vimentin 表达提高 2-3 倍,迁移与侵袭能力增强 4-5 倍。赛吉生物 DARC-G 系统模拟实验证实,这种 EMT 过程与缺氧诱导因子 HIF-1α 的激活密切相关。
化疗耐药机制:微重力培养的肿瘤球中,ABC 转运蛋白家族表达提高 2-4 倍,导致紫杉醇、顺铂等化疗药物的 IC50 值增加 3-5 倍。研究发现,微重力通过激活 PI3K/Akt 通路增强肿瘤细胞的药物外排能力,为克服耐药性提供了新靶点。肿瘤干细胞富集:微重力环境可使肿瘤干细胞比例从 5% 提高至 20%,其自我更新能力增强,对放疗的抵抗性提高 60%,这一发现为肿瘤复发机制研究提供了重要线索。
六、药物研发与递送系统优化
核心方向:利用微重力独特环境,优化药物筛选模型,提高药物研发效率;探索微重力对药物递送系统的影响,开发高效靶向给药策略。
前沿进展:药物筛选效率提升:微重力 3D 肿瘤模型的药物反应与临床疗效相关性达 80%(2D 模型仅 50%),可显著降低临床前研究的假阳性率。赛吉生物 MFBS 类器官芯片微重力模拟器结合微流控技术,实现了药物浓度梯度的精准控制,筛选效率提高 5 倍。
核酸药物递送增强:中国空间站实验证实,微重力下细胞对脂质纳米颗粒(LNP)包裹的 mRNA 摄取效率提高 3 倍,蛋白表达水平增加 5 倍,为核酸药物研发提供了新策略。机制研究表明,微重力降低细胞膜流动性,促进内吞体逃逸,提高 mRNA 释放效率。纳米药物载体优化:微重力环境下制备的聚合物纳米粒粒径分布更均匀(PDI<0.1),药物包封率提高 20%-30%,体内循环时间延长 2 倍,显著增强抗肿瘤效果。
七、技术支撑体系:地面微重力模拟设备的创新
空间在轨实验成本高昂(单次任务 > 10 亿元)、周期有限(通常 < 30 天),地面精准模拟设备成为微重力科研快速迭代的核心支撑,呈现三大技术发展趋势:
1.精准化模拟技术
苏州赛吉生物 DARC-P 灌流微重力模拟系统采用二轴 3D 回转结构,实现 10⁻³g 级微重力精准模拟,转速调节增量≤0.1 RPM,确保实验可重复性。随机变速回转与恒速回转双模式设计,适配细胞培养、组织工程等不同实验场景,解决通用设备难以满足个性化课题的痛点。
2.定制化与模块化设计:
PMSP 全生命周期植物微重力模拟培养舱采用 “核心基础模块 + 定制拓展模块" 架构,可加装根系观测、精准滴灌等功能模块,无需整体更换设备即可实现研究方向延伸。DARC-G 系统支持 0.001g-1g 重力范围精准调节,适配月球(0.17g)、火星(0.38g)等特殊重力环境研究。
3.多技术融合集成:MFBS 类器官芯片微重力模拟器将重力调控与微流控灌流动态耦合,可动态调节流体剪切力(0.2-2 dyn/cm²),模拟体内不同器官的力学微环境。实时成像与数据分析系统联动,可追踪细胞在微重力下的生长动态,为解析生理响应提供精准数据支撑。
八、未来展望与挑战
核心挑战:重力信号转导的分子机制尚未阐明,缺乏精准调控靶点;地面模拟与真实空间微重力存在差异(如 g-jitter 效应),影响实验结果的外推性;微重力效应的个体差异显著,增加了航天医学防护的复杂性。前沿方向多组学整合研究:结合单细胞测序、蛋白质组学、代谢组学技术,系统解析微重力对细胞的分子调控网络;重力响应基因编辑:利用 CRISPR-Cas9 技术编辑重力敏感基因,探索增强细胞抗微重力能力的新策略;跨尺度研究:从分子 - 细胞 - 组织 - 器官水平,构建微重力效应的完整调控通路,为航天医学防护与地面疾病治疗提供全面解决方案。
转化应用前景:
微重力培养的 3D 类器官模型将成为药物研发的标准平台,显著提高临床转化效率;
微重力增强的干细胞治疗技术有望应用于骨关节炎、脊髓损伤等疾病;
基于微重力机制的抗肌weisuo、骨质疏松药物开发,将惠及航天与地面两大人群。
微重力环境下细胞生物学研究的主要方向与前沿进展:结语:微重力细胞生物学研究正处于从现象观察到机制解析、从基础研究到转化应用的关键阶段。中国空间站的建成与国产精准微重力模拟设备(如苏州赛吉生物 DARC 系列)的研发,为该领域提供了强大的技术支撑。未来,随着研究的深入与技术的突破,微重力环境不仅将助力人类探索太空,更将为地面生命健康保障带来革命性变化。

咨询:苏州赛吉生物